
Kanserli hücrelerdeki bozukların tanımlanması sonrasında bozulmuş yapılara yönelik veya onların etkilerini ortadan kaldırmaya yönelik seçici olarak kanser hücrelerini hedefleyen tedavilerdir.
İlacın akıllı ilaç, hedefe yönelik ilaç kategorisinde değerlendirilebilmesi için kanser biyolojisinin ortaya konmuş olması gerekmektedir. Akıllı ilaçlarla hedefe yönelik tedaviler başlangıçta az sayıda kanser ilişkili molekülü değerlendirerek yapılmaktaydı. Ancak günümüzde kanser hücrelerinin farklı mutasyonları ve bozulmuş yolakları olabileceği ortaya konmuştur.
Bu nedenle kanserde akıllı ilaç veya hedefe yönelik tedaviler veya immünoterapi planlanması durumunda mutlaka kanser biyolojisinin ortaya konması ve bu değişen biyolojinin çözümlenmesi sonucunda tedavi planlanmalıdır.
Kişiye özel kanser tedavi merkezinde yüksek oranda akıllı ilaçlar tedaviler planlanmaktadır. Bazen tek bir ilaç kullanılırken daha sıklıkla bir kaç ilaç kombinasyon halinde kullanılmaktadır. Kombinasyon tedavileri ile daha başarılı sonuçlar alınabilmektedir.
Aynı şekilde immünoterapi, akıllı ilaç kombinasyonları ve bunlara İntegratif tedavilerinde eklenmesi gerekebilmektedir.
Kapsamlı genomik haritalama akıllı ilaç kullanacak her hastada neredeyse olmazsa olmaz noktadadır. Bazen hangi tedaviyi yapacağınızı bilmek yanında hangi tedaviyi yapmayacağınızı da bilmek çok önemlidir. Yaptığınız tedavinin direnç yollarını görmek ve ona göre önlem almak gerekmektedir.
Akıllı ilaç olarak tanımlanan moleküllerin genellikle tek bir hedefleri yoktur. Birden fazla molekülle etkileşebilmektedirler. Ancak belirli moleküllere bağlanan ilaçlarda mevcuttur. Hastanın değişen biyolojisinin bilinmesi özellikle çoklu moleküle bağlanan akıllı ilaçların kullanımında önemlidir.
İlaç firmaları tarafından yaklaşık 10 yıldır sadece hedefe yönelik akıllı moleküller ve immünoterapi ilaçları geliştirilmektedir. Bu nedenle her yıl bir çok yeni akıllı molekül insanlığın kullanımına sunulmaktadır. Artan molekül sayısı ve hedef nedeniyle kanser biyolojisinin ortaya konularak tedavinin kişiselleştirilmesi daha da önem arzetmektedir.
Yakın zamanda Sotorasib, belzutifan gibi ilaçlar daha spesifik hedeflere yönelik olarak insanlığın kullanımına sunulmuştur.
Sotorasib KRAS G12C mutasyonlarında etkilidir. Aşağıdaki şekilde de olduğu üzere Sotorasib KRAS G12C mutasyonunun neden olduğu protein bölgesine bağlanarak sürekli aktif olan bu mutasyonu etkisiz hale getirebilmektedir.
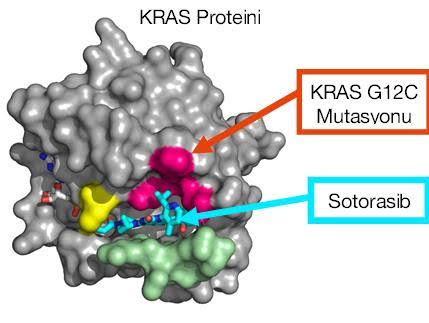
Belzutifan ise VHL geninin fonksiyon kaybına neden olan mutasyonlarda.
Belzutifan ise VHL fonksiyon kaybı sonrası artan HIF-2alfa molekülünü hedeflemektedir. Görüldüğü üzere iki ilaç arasında hedef açısından farklılıklar vardır. Bazen bozulan proteinin neden olduğu değişiklikler hedeflenirken bazen direkt bozulan proteinler hedeflenebilmektedir.
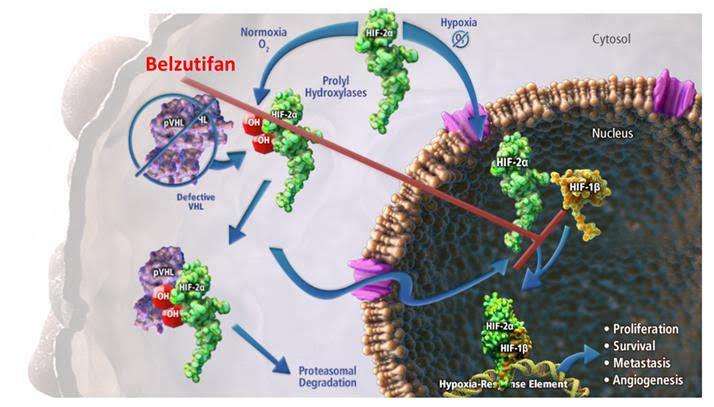
En önemli kanser yolaklarından bir tanesi MAPK yolağıdır. Bir çok kanserde bu yolakta bozukluk bildirilmiştir. Bu yolaktaki bozukluklar kanserin hızla yayılmasına büyümesine neden olmaktadırlar.
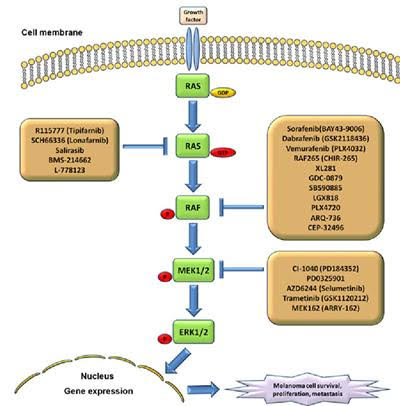
Sarı kutucukların içinde MAPK yolarının o seviyesine etkili olan geliştirilmiş ve geliştirmekte olan ilaçların listesini görmektesiniz. Bu yolakta çok sayıda mutasyon olabilmektedir. Mutasyonun ne olduğu hangi yolaklarla ilişkili olduğu da önem taşımaktadır. Görüldüğü üzere tek bir ilaç yoktur ve kanser biyolojisi analiz edilmeden karar verilmesi uygun olmayacaktır.
Yukarıdaki şekli hücrenin içindeki mekanizmaları ve yolakları ve bunların birbirleri ile olan ilişkilerini görebilmeniz için koydum. Neden kapsamlı genomik haritalama yapılmalıdır neden değişen kanser biyolojisi çözümlenmelidir daha net anlaşılmaktadır.
Tek bir molekülle kanseri tedavi etmek çoğunlukla pek mümkün değildir. Kombinasyon tedavileri oluşturulmalıdır.
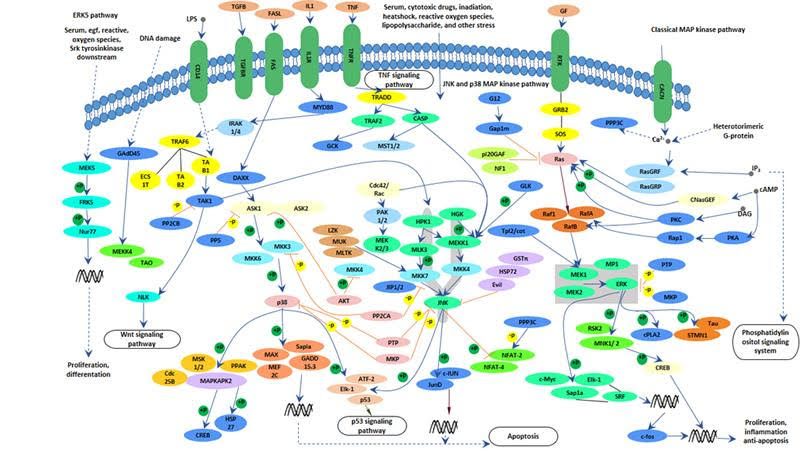
Akıllı ilaç öncelikle akıllı bir dizaynla olabilmektedir, akıllı bir dizayn için değişen kanser biyolojisinin analiz edilmesi gerekmektedir.
Daha başarılı tedaviler daha iyi bilgi ve analizle mümkün olabilmektedir.
Akıllı molekülleri akıllıca kullanırsanız etkilerini görebilirsiniz.